.jpg)
Terapia con medicación
Soporte vital pediátrico avanzado
Mayo 2013
Apartado 7
Manejo del shock
Descripción general
Una vez que identifique el shock en un niño enfermo o lesionado, una
intervención temprana puede reducir la morbilidad y la mortalidad. En este
apartado se tratan los objetivos y las prioridades en el manejo del shock, los
aspectos básicos de tratamiento, el manejo general y avanzado, así como el
manejo específico según la etiología.
Objetivos de aprendizaje
Después de estudiar este apartado podrá :
Describir los objetivos generales del manejo del shock, entre otros: prioridades de tratamiento inicial, monitorización y continuación del manejo
Describir la reanimación efectiva con líquidos
Tratar el shock según el tipo y la gravedad
Resumir los principios de manejo intensivo del shock obstructivo, cardiogénico, distributivo e hipovolémico
Preparativos para el curso
Durante
el curso, tendrá que tratar a un niño en shock. Para ello, deberá conocer los
tratamientos específicos y generales para los distintos tipos de shock.
Objetivos del manejo del shock
Los objetivos del tratamiento del shock son mejorar la administración de O2, el
equilibrio entre perfusión tisular y requerimiento metabólico, revertir los
efectos de anomalías en la perfusión, restaurar la función de los órganos y
evitar la progresión a paro cardíaco. La rapidez de intervención es crucial:
solo con los conocimientos necesarios que permitan identificar el shock y la
competencia en las habilidades pertinentes para una respuesta rápida habrá
opciones para salvar la vida del paciente. Cuanto más se retrase el inicio de la
reanimación desde el primer signo del problema y la restauración de la
administración de O2 adecuada y la perfusión de los órganos, peor será el
resultado. Cuando el niño entra en paro cardíaco, el pronóstico es muy
desfavorable.
Signos de alarma
Identifique signos que alerten que los mecanismos compensatorios no están
funcionando bien en un niño con enfermedades o lesiones graves. Cuando advierta
un agravamiento en el estado del niño, actúe con determinación coordinándose con
el equipo de reanimación para aplicar un tratamiento efectivo. Los signos de
alarma que indican progresión de shock compensado a hipotenso incluyen :
Taquicardia más acusada
Pulsos periféricos débiles o no palpables
Pulsos centrales débiles
Acortamiento de la presión diferencial
Extremidades distales frías con llenado capilar prolongado
Menor nivel de consciencia
Hipotensión (signo visible en las últimas fases de la progresión)
Cuando el niño está hipotenso, la perfusión de los órganos suele quedar bastante
afectada y podría presentarse disfuncián orgánica incluso si no hay progresión a
paro cardíaco.
Aspectos básicos del manejo del shock .
|
Identificar e intervenir |
La identificación rápida del shock compensado es decisiva para un tratamiento efectivo y un buen resultado. |
El tratamiento intensivo del shock se centra en restablecer la administración de
O2 a los tejidos y mejorar el equilibrio entre requerimiento metabólico y
perfusión tisular. El tratamiento intensivo del shock consiste
en :
Optimizar el contenido de O2 de la sangre
Mejorar el volumen y la distribución del gasto cardíaco
Reducir la demanda de O2
Corrección de las alteraciones metabólicas
Intente identificar y anular la causa subyacente del shock a la vez que inicia
intervenciones rápidas.
Optimización del contenido de oxígeno de la sangre
El contenido de O2 en sangre se determina mediante la oxigenación de hemoglobina
y concentración de hemoglobina.
Para optímizar el contenido de O2 :
Administre una alta concentración de O2 (use una mascarilla de no reinhalación para administrar O2 al 100%)
Use ventilación mecánica invasiva o no invasiva para mejorar la oxigenación corrigiendo el desequilibrio de ventilación/flujo sanguíneo 0//0) u otro trastorno respiratorio
Si la concentración de hemoglobina es baja, considere la posibilidad de una transfusión de concentr~po de globulos rojos (PBRC)
Mejora del volumen y distribución del gasto cardíaco
Las medidas para mejorar el volumen y la distribución del gasto cardíaco
dependen del tipo de shock :
Hipovolémico
Distributivo
Cardiogénico
Obstructivo
Shock hipovolémico
La administración rápida de líquidos cristaloides isotónicos está indicada en la
mayoría de niños que presentan signos y síntomas de shock hipovolémico.
Considere los signos vitales y la exploración física para evaluar la respuesta
del niño a
cada
bolo de líquidos. Busque evidencias persistentes de hipovolemia o pérdida de
líquido para determinar si es necesario administrar más líquidos
Shock distributivo
Sospeche de un shock distributivo si hay evidencias de resistencia vascular
sistémica baja (RVS, aumento de la presión diferencial) y mala distribución del
flujo sanguíneo (p. ej.: vasodilatación y piel caliente). Aunque el result?J,do
final es una administración inadecuada de O2 a los órganos, la principal
anomalía es una baja RVS debida a la respuesta a los organismos invasores (p.
ej.: sepsis) o a la pérdida de tono vasomotor (p. ej.: anafilaxia o lesión de
médula espinal) y aumento de la permeabilidad capilar.
El manejo del shock distributivo está dirigido al restablecimiento rápido del
volumen intravascular para mejorar el llenado del espacio vascular vasodilatado.
Si la hipotensión persiste a pesar de la administración de líquidos, considere
los vasopresores para combatir el principal problema de escasa RVS. Aunque el
gasto cardíaco suele aumentar al principio del shock distributivo, si hay signos
de disfunción miocárdica, use agentes inotrópicos para mejorar la contractilidad
cardíaca.
Shock cardiogénico
Sospeche de shock cardiogénico ante signos de perfusión deficiente y congestión
venosa sistémica o pulmonar (p. ej.: aumento del esfuerzo respiratorio,
respiraciones con quejidos, ingurgitación yugular o hepatomegalia). Además,
piense en la posibilidad de un shock cardiogénico si hay un deterioro clínico en
la perfusión y función respiratoria en respuesta a la reanimación con líquidos.
Si los signos son propios de un shock cardiogénico, en lo posible, centre el
tratamiento en mejorar el gasto cardíaco a la vez que se reduce el requerimiento
metabólico. Los tratamientos específicos pueden incluir ventilación con presión
positiva invasiva o no invasiva para reducir el esfuerzo respiratorio y mejorar
la oxigenación. Considere una infusión lenta de líquido por vía IV en una
proporción de 5 a 10 ml/kg de 10 a 20 minutos, observando con especial
detenimiento por si se llegaran a presentar signos de deterioro. El paso al
tratamiento con agentes vasodilatadores e inotrópicos se determinará según la
necesidad de mantener la presión arterial, restablecer la perfusión tisular o
minimizar los efectos adversos de los inotrópicos en la demanda de O2
miocárdico. Consulte la sección "Terapia con medicación" más adelante en este
apartado.
Se recomienda consultar al experto en las primeras fases del tratamiento de
niños con shock cardiogénico. La selección del mejor fármaco vasoactivo se
establecerá
según los datos obtenidos con el ecocardiograma u otras pruebas. Los niños
pueden beneficiarse del tratamiento con vasodilatadores, inotrópicos o
inodilatadores para reducir la poscarga, mejorar la contractilidad y aumentar el
flujo sanguíneo a los órganos vitales.
Shock obstructivo
Sospeche de shock obstructivo si el niño muestra signos de presión venosa
central alta, congestión venosa con perfusión deficiente periférica y desarrollo
rápido de hipotensión. Mantenga la función cardiovascular (p. ej.: con
administración de bolo de líquidos y posibles agentes vasoactivos) mientras
sigue evaluando, obtiene pruebas diagnósticas y consulta a personal experto. La
clave del manejo del shock obstructivo es identificar y tratar la causa
rápidamente.
Reducción de la demanda de oxígeno
En todas las formas de shock, intente mejorar el equilibrio entre el consumo y
el aporte de O2 usando medidas para reducir la demanda de O2, Los factores más
comunes que contribuyen a aumentar la
demanda de O2 son :
Mayor esfuerzo respiratorio
Dolor y ansiedad
Fiebre
Mantenga la respiración con ventilación no invasiva o intubación endotraqueal y
ventilación asistida. Para facilitar la intubación y la ventilación mecánica,
podría tener que administrar sedantes o analgésicos y bloqueo neuromuscular.
Controle el dolor y la ansiedad con analgésicos y sedantes. Use los sedantes y
analgésicos con precaución; pueden suprimir la respuesta endógena a la
sobrecarga e impedir los mecanismos compensatorios como la taquicardia. Controle
la fiebre administrando antipiréticos y
otras medidas para bajar la temperatura.
Corrección de las alteraciones metabólicas
Muchos estados que desencadenan el shock podrían ocasionarse o complicarse por alteraciones metabólicas como :
Hipoglucemia
Hipocalcemia
Hiperpotasemia
Acidosis metabólica
Todas estas
condiciones pueden afectar de forma adversa a la contractilidad cardíaca. La
acidosis metabólica es característica de todas las formas de shock.
La
hipoglucemia es
un nivel de glucosa en suero bajo. La glucosa es vital para la correcta función
cardíaca y cerebral. Los niveles de glucosa pueden ser bajos en
lactantes y niños con enfermedad crónica. Si la hipoglucemia se deja sin tratar
pueden aparecer convulsiones y lesiones cerebrales.
La
Hipocalcemia es
una concentración baja de calcio en plasma ionizado en suero. El calcio es
esencial para una función
cardíaca
y
tono vasomotor óptimos.
La
Hiperpotasemia es
una concentración elevada de potasio sérico
que puede deberse a una insuficiencia renal, muerte
celular
,
dosificación excesiva de fármacos o acidosis. La acidosis
produce un desplazamiento del potasio desde el
nivel intracelular hasta el extracelular, incluido el espacio intravascular.
Como resultado, la acidosis puede producir una elevación en el potasio sérico.
La acidosis metabólica se
desarrolla por la producción de ácidos, como ácido láctico, cuando la perfusión
tisular no es adecuada. La disfunción renal o gastrointestinal puede causar
acidosis metabólica. La disfunción renal puede
causar la retención de ácidos orgánicos o la pérdida de
iones de bicarbonato. La disfunción gastrointestinal, como
la
diarrea, puede provocar la pérdida de iones de bicarbonato. Si la acidosis
metabólica es grave, la contractilidad miocárdica podría resultar afectada y
reducir el efecto de los vasopresores. A menos que la acidosis metabólica se
deba únicamente a la pérdida de bicarbonato, no responde bien al tratamiento con
amortiguadores. Trate la acidosis intentando restablecer la perfusión tisular
con reanimación por líquidos y agentes vasoactivos. Si el tratamiento es eficaz,
la acidosis metabólica desaparecerá.
En ocasiones, podría ser necesario recurrir a los amortiguadores (p. ej.:
bicarbonato sódico) para corregir totalmente la acidosis metabólica aguda que
dificulta la función de los órganos vitales. El bicarbonato sódico actúa por la
combinación de iones de hidrógeno (ácidos) que producen dióxido de carbono
yagua; el dióxido de carbono se elimina mediante un aumento de la ventilación
alveolar. La ventilación asistida siempre es importante en niños
con una enfermedad grave, pero resulta especialmente importante si la acidosis
metabólica se trata con bicarbonato sódico.
La corrección de las alteraciones metabólicas podría ser esencial para optimizar
la función de los órganos. Mida la concentración de calcio ionizado (forma
activa de calcio en el cuerpo) y la glucemia. Reponga según resulte indicado.
Considere administrar bicarbonato sódico para tratar la acidosis metabólica refractaria
a los intentos de aumento del gasto cardíaco o redistribución del flujo
sanguíneo a los órganos vitales.
Criterios de valoración terapéutica
Ningún criterio de valoración de la reanimación se ha identificado como un
indicativo común de una perfusión tisular y homeostasis celular adecuadas.
Los signos que indican una mejoría clínica hacia un estado hemodinámico normal son :
Frecuencia cardíaca y presión arterial normales para el grupo de edad
Pulsos normales
Tiempo de llenado capilar < 2 segundos
Extremidades calientes
Estado mental normal
Diuresis > 1 ml/kg por hora
Disminución del lactato sérico
Reducción del déficit de base
Saturación de oxígeno venoso central (ScVod > 70%)
Controle estos criterios de valoración terapéutica además de tratar la causa
subyacente del shock del niño.
|
Dato fundamental |
Aunque la presión arterial se mide fácilmente, es importante evaluar otros parámetros clínicos para evaluar la perfusión tisular. Recuerde que la presión arterial puede ser normal en niños con shock grave, y que con la presión arterial no invasiva se podría obtener una medición inexacta en caso de perfusión deficiente. |
Manejo general del shock
Componentes del manejo general
El manejo general del shock consiste en las siguientes acciones (tenga en cuenta
que el equipo podría ejecutar varias de estas intervenciones a la vez) :
Posicionamiento adecuado
Vía aérea y ventilación
Acceso vascular
Reanimación con líquidos
Monitorización
Reevaluación frecuente
Pruebas de laboratorio
Terapia con medicación
Consulta al subespecialista
Posicionamiento adecuado
El manejo inicial del shock incluye la posición del niño con enfermedades o
lesiones graves. Si el niño está consciente y está hemodinámicamente estable,
deje que se coloque en la posición que le resulte más cómoda (p. ej.: sentado,
en brazos del cuidador); así se tranquilizará y podrá proceder con la impresión
inicial y evaluación primaria. Sí el niño está hipotenso y la respiración se ve
comprometida, coloque al niño en la posición de Trendelenburg (decúbito supino,
con la cabeza 30° más baja que los pies).
Vía aérea y ventilación
Mantenga una vía aérea permeable y facilite la respiración.
Administre una concentración alta de O2 adicional a los niños con shock. Por lo
general, el mejor método es un sistema de suministro de alto flujo de O2,
Algunas veces, la administración de O2 tiene que combinarse con ventilación
asistida si las respiraciones no son efectivas, el estado mental está afectado o
el esfuerzo respiratorio ha aumentado considerablemente. Las intervenciones
apropiadas pueden incluir ventilación mecánica o presión positiva no invasiva en
la vía aérea tras la intubación endotraqueal.
Acceso vascular
Cuando
la vía aérea esté permeable y la respiración esté mantenida, obtenga un acceso
vascular para la reanimación con líquidos y la administración de medicación. En
el shock compensado, está indicado intentar con una cánula de vía venosa
periférica. En el shock hipotenso, obtener un acceso vascular inmediato es
crítico y el mejor método es eloacceso 10 si el acceso IV periférico no es
posible. Según la experiencia del proveedor y las circunstancias clínicas, el
acceso venoso central podría resultar útil. No obstante, para el acceso venoso
central es necesario más tiempo que para la colocación de una vía IO.
Para obtener más información sobre el acceso I0, consulte "Acceso intraóseo" en "Recursos para el manejo de las emergencias circulatorias" al final de este apartado.
|
Concepto crítico Acceso intraóseo |
Si el acceso vascular periférico no es posible en niños con shock hipotenso o compensado, dispóngase a establecer un acceso IO. |
Reanimación con líquidos
Cuando
el acceso vascular se haya establecido, inicie de inmediato la reanimación con
líquidos.
|
Dato fundamental |
Inyecte un bolo de 20 ml/kg de solución cristaloide isotónica durante 5 a 20 minutos. Reevalúe* y repita con bolos de 20 ml/kg para restablecer la presión arterial y la perfusión tisular.
|
Monitorización
Evalúe la efectividad de la reanimación con líquidos y el tratamiento con
medicación mediante monitorización frecuente o continua de los siguientes
parámetros :
Saturación de O2 utilizando oximetría de pulso (SpO2)
Frecuencia cardíaca
Presión arterial y presión diferencial
Estado mental
Temperatur
Diuresis
En cuanto sea posible, inicie la monitorización no invasiva (SpO2 ,
frecuencia cardíaca, presión arterial). Evalúe el estado mental. Mida la
temperatura y diuresis con una sonda vesical permanente. Considere la
monitorización invasiva (p. ej.: catéter venoso central y arterial), según la
experiencia del proveedor y los recursos disponibles.
|
Concepto crítico Monitorice para evaluar tendencias |
El estado de un niño en shock es dinámico. La monitorización continua y las reevaluaciones frecuentes son determinantes para evaluar tendencias en el estado del niño e identificar la respuesta al tratamiento. |
Reevaluación frecuente
Reevalúe frecuentemente el estado respiratorio, cardiovascular y neurológico del niño para :
Evaluar tendencias en el estado mdel niño
Determinar las respuestas al tratamiento
Planificar las siguientes intervenciones
Un niño en shock está en un estado clínico dinámico que puede empeorar en cualquier momento requiriendo intervenciones para salvar la vida como intubación endotraqueal. Continúe con las reevaluaciones frecuentes hasta que el niño se estabilice ó se traslade a la unidad de Cuidados Avanzados.
Pruebas de laboratorio
Las pruebas de laboratorio ofrecen información importante que le ayudará a :
Identificar la etiología y gravedad del shock
Evaluar la disfunción orgánica asociada al shock
Identificar alteraciones metabólicas
Evaluar la respuesta al tratamiento
Consulte el apartado 11: "Manejo posparo cardíaco" para obtener información adicional sobre la evaluación de la función de los órganos vitales. Considere también la consulta al experto para el diagnóstico y manejo de insuficiencia de los órganos vitales.
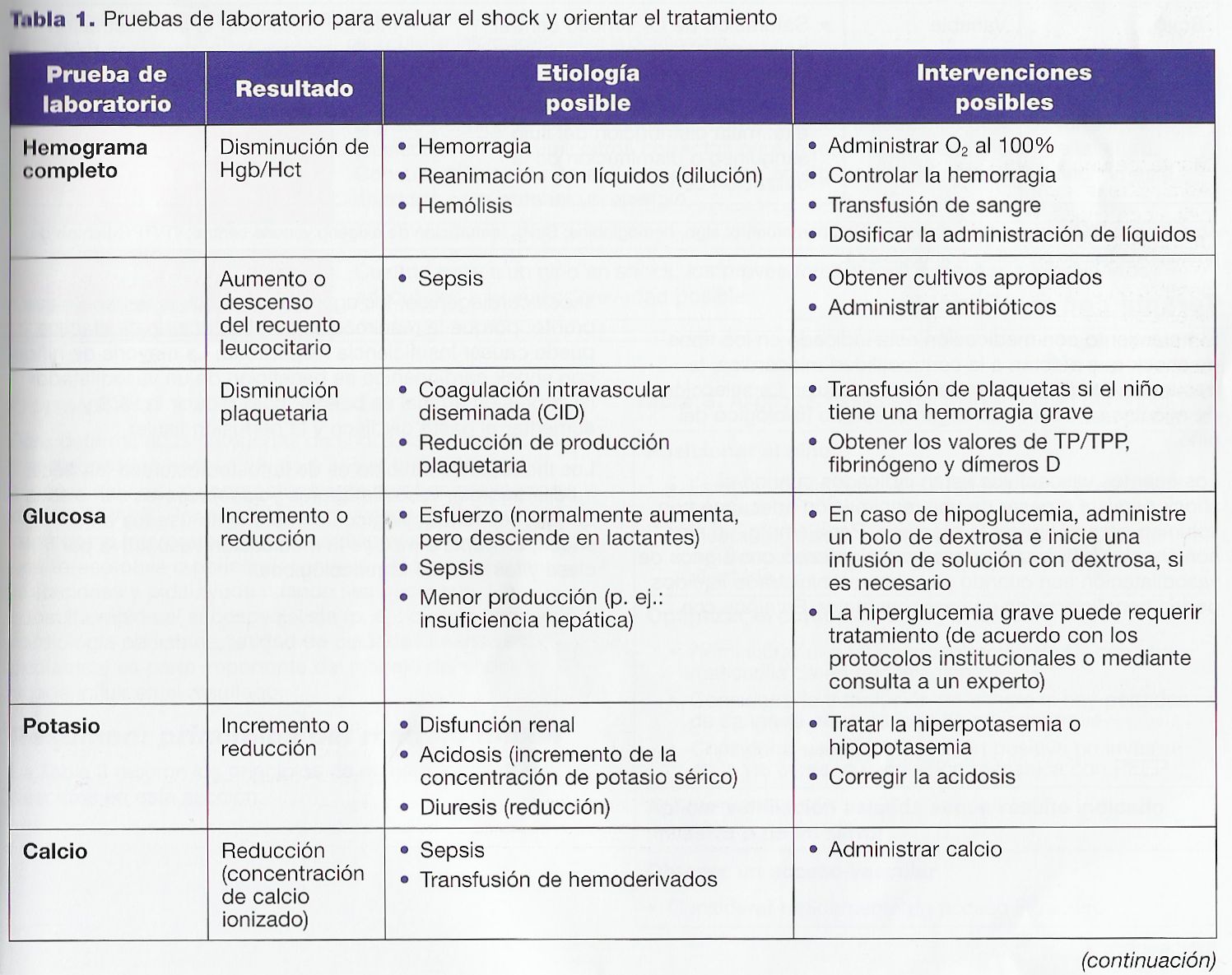
La Tabla 1 presenta algunas pruebas de laboratorio que pueden ayudarle a
identificar la etiología y gravedad del shock y orientar el tratamiento.

.jpg)
Terapia con medicación
El tratamiento
con medicación está indicado en los tipos de shock que afectan a la
contractilidad miocárdica, la frecuencia cardíaca y la resistencia vascular. La
selección de agentes se determina según el estado fisiológico del niño.
Los agentes vasoactivos están indicados cuando el shock persiste a pesar de una
reanimación adecuada con volumen para optimizar la precarga. Por ejemplo, un
niño con shock séptico que permanece hipotenso con signos de vasodilatación aun
cuando se le han administrado líqtJidos podría beneficiarse de un
vasoconstrictor. En niños con shock cardiogénico, los agentes vasoactivos deben
usarse pronto, porque la reanimación con líquidos no es efectiva y puede causar
insuficiencia respiratoria. La mayoría de niños con shock cardiogénico se
benefician de un vasodilatador (si la presión arterial es buena), para reducir
la RVS y aumentar el gasto cardíaco y la perfusión titular.
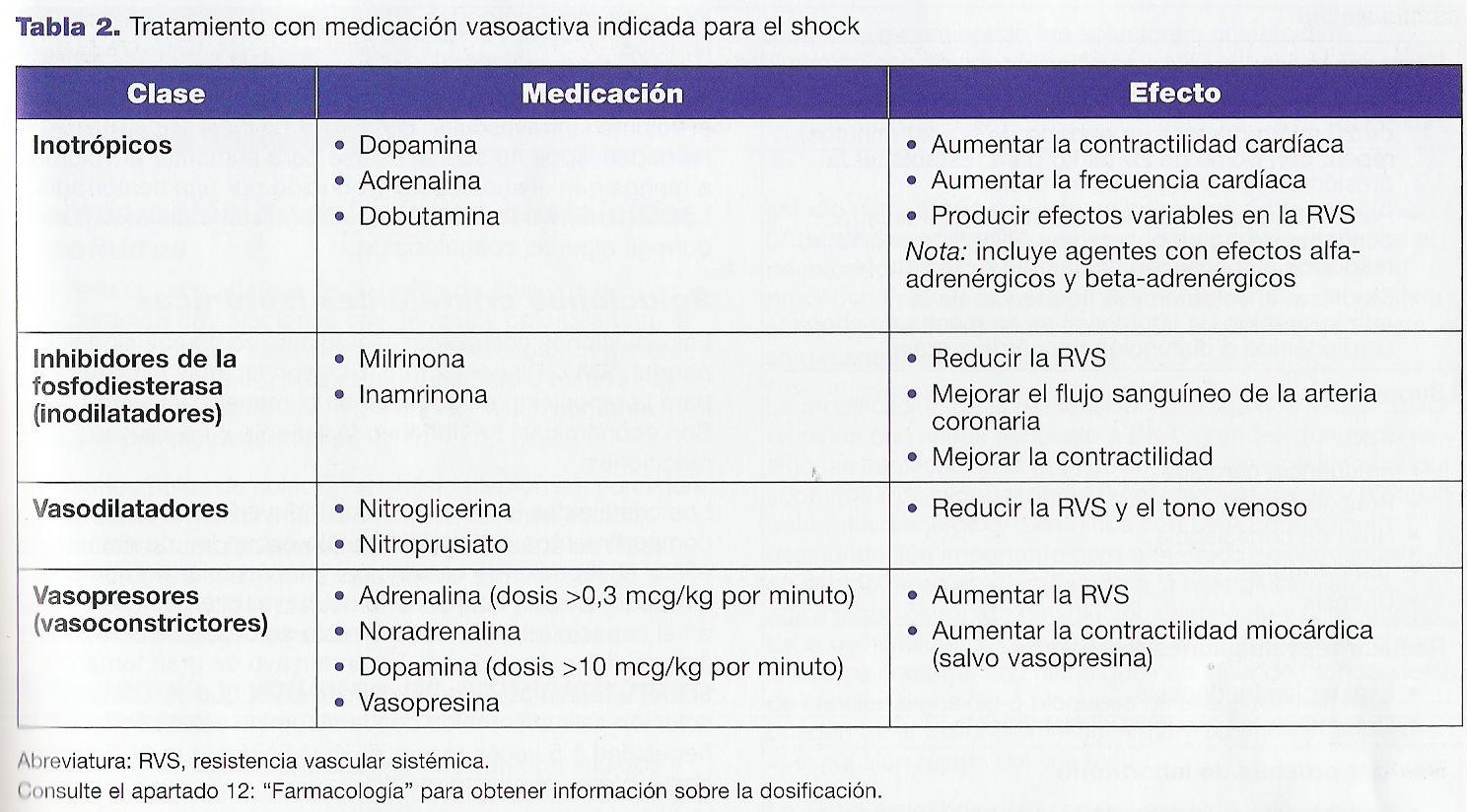
Los inotrópicos, inhibidores de la fosfodiesterasa (es decir, inodilatadores),
vasodilatadores y vasopresores son clases de agentes farmacológicos comúnmente
usados en el shock.
La Tabla 2 incluye la medicación vasoactiva por clase y los efectos farmacológicos.
|
Concepto crítico Cinta con códigos de color basada en la talla del paciente |
Use una cinta con códigos de color basada en la talla del paciente
para determinar el peso del niño (si no se conoce); podrá entonces
calcular las dosis de fármacos y seleccionar los suministros
correctos para la reanimación en función de la altura. Consulte
"Recursos para el manejo de las emergencias circulatorias" al final
de este apartado para obtener un ejemplo. |
|
Concepto crítico Consulta al experto |
Cuando trate a un niño en shock, los proveedores deben consultar a los expertos adecuados a la mayor brevedad posible. |
Consulta al
subespecialista
Para determinadas categorías de shock, las intervenciones y el diagnóstico necesarios para salvar una vida pueden escapar del nivel de competencia de muchos proveedores de SVAP/PALS. Por ejemplo, un proveedor quizá no sepa cómo interpretar una ecocardiografía o realizar una toracotomía o pericardiocentesis. Reconozca sus limitaciones y pida ayuda cuando sea necesario.
Una consuIta rápida al subespecialista (p. ej.: cirugía pediátrica, cardiología
pediátrica, unidad de cuidados intensivos pediátrica) es parte importante del
manejo del shock y puede influir en el resultado.
Resumen: principios
del manejo inicial
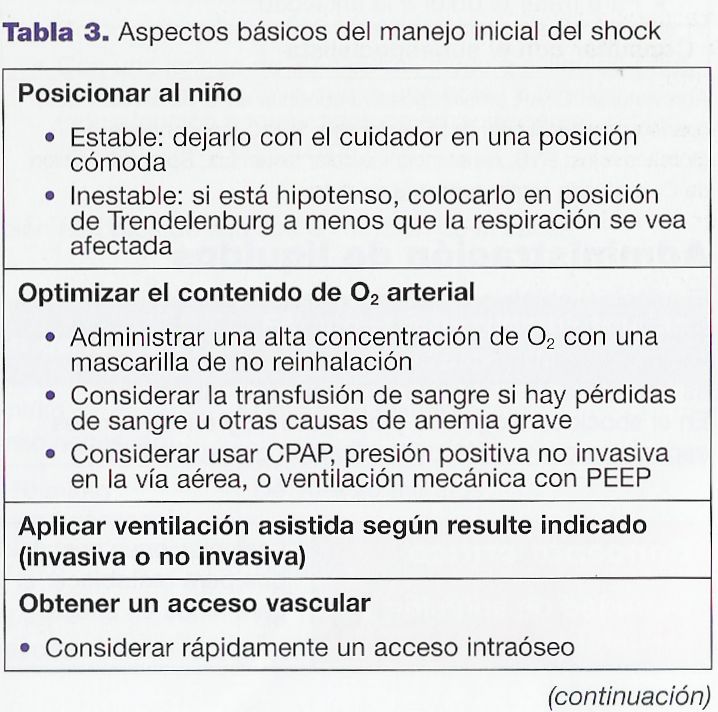
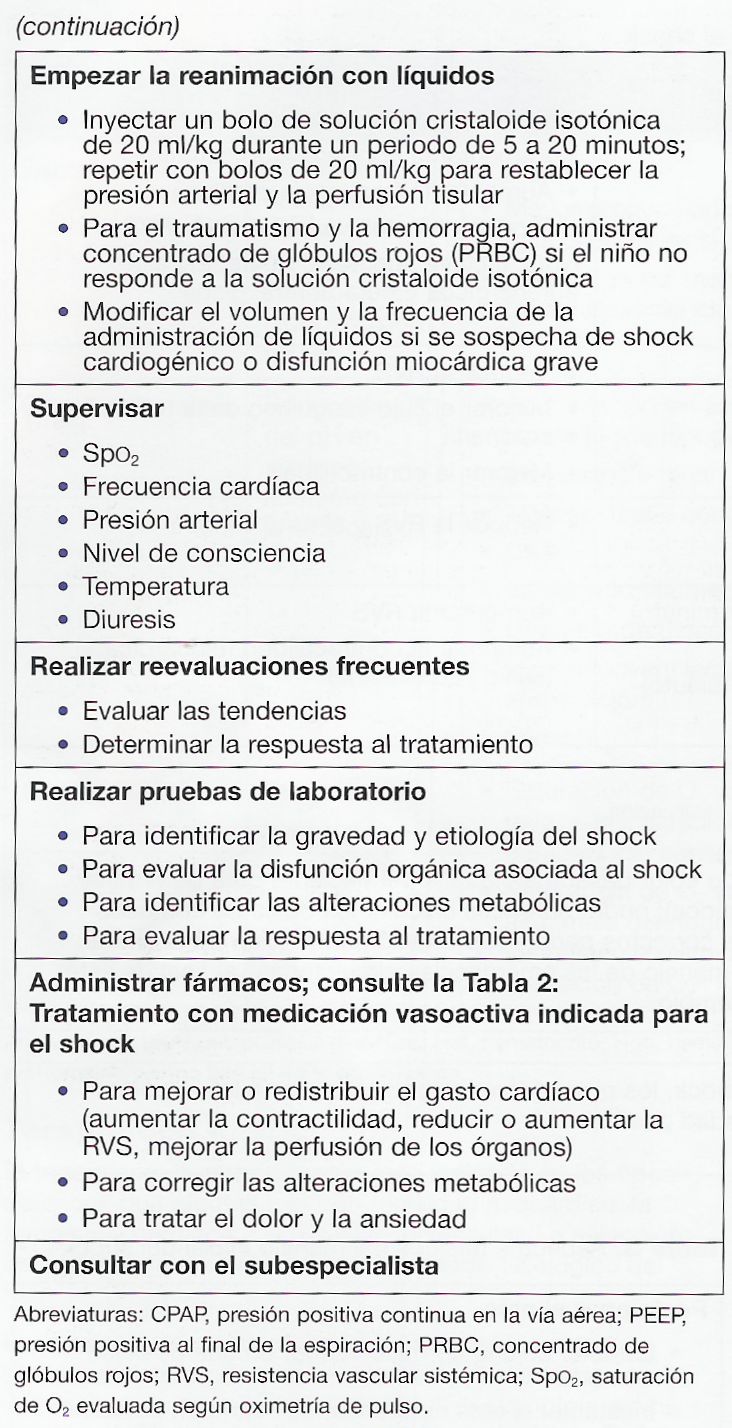
La tabla 3
resume los principios de manejo inicial del shock descritos
en esta sección.
Administración de
líquidos
El principal objetivo de la administración de líquidos en el shock es
restablecer el volumen intravascular y la perfusión tisular. La reanimación
rápida y enérgica con líquidos es necesaria en el shock hipovolémico y
distributivo.
En el shock cardiogénico y obstructivo, y en afecciones especiales como DKA o intoxicación grave, podrían indicarse otros enfoques que no sean la administración de líquidos.
Las soluciones coloides y cristaloides isotónicas aumentan el volumen
intravascular. En niños, la sangre y los hemoderivados no suelen usarse para
aumentar el volumer a menos que el shock esté producido por una hemorragia. Los
hemoderivados también podrían estar indicados para corregir algunas
coagulopatías.
Soluciones cristaloides isotónicas
Las soluciones cristaloides isotónicas, como solución salina normal (SN) o
Ringer lactato (RL), son las más indicadas para la reposición de volumen en el
manejo del shock. Son económicas, se obtienen fácilmente y no causan reacciones.
Los cristaloides isotónicos se distribuyen a través de los compartimentos
extracelulares. No expanden de manera eficaz el espacio (de circulación)
intravascular porque solo alrededor de una cuarta parte de su volumen permanece
en el espacio intravascular; el resto se desplaza al espacio (intersticial)
extravascular. En un ensayo de gran tamaño sobre la reanimación con volumen en
el que se comparó la solución salina isotónica con la albúmina se observó una
necesidad 1,5 veces mayor de cristaloides que de coloides para obtener el mismo
efecto.
Un niño sano puede tolerar bien la infusión rápida de un volumen grande de
líquido, pero en un niño con una enfermedad grave y con insuficiencia renal o
cardiopatía podría aparecer edema periférico y pulmonar.
|
Concepto crítico Cantidad de solución cristaloide |
Las soluciones cristaloides isotónicas se distribuyen por el espacio extracelular, por lo que para restablecer el volumen intravascular puede ser necesario una gran cantidad para niños en shock. |
Soluciones coloides
Las soluciones coloides (p. ej.: 5% de albúmina, plasma fresco congelado y
expansores sintéticos de plasma, como hetastarch, dextrán 40 y dextrán 60)
contienen moléculas relativamente grandes que permanecen en el espacio
intravascular durante más horas que las soluciones cristaloides isotónicas. Por
tanto, son expansores más, eficaces del volumen intravascular.
No obstante, las soluciones coloides pueden tener desventajas para la
reanimación intensiva de un niño en shock. No se obtienen tan fácilmente como
las soluciones cristaloides y su preparación requiere tiempo.
Las soluciones coloides de hemoderivados pueden causar reacción. Los coloides
sintéticos pueden causar coagulopatías; su uso se suele limitar a 20 ó 40 ml/kg.
Como con las soluciones cristaloides, una administración excesiva de coloides
puede producir edema pulmonar, especialmente en niños con insuficiencia renal o
cardiopatía.
|
Dato
fundamental : |
En la mayoría de niños con shock, se recomiendan las soluciones cristaloides isotónicas para iniciar la reanimación con líquidos. |
Comparación de soluciones cristaloides y coloides
Ls resultados y análisis de décadas de ensayos de comparación de soluciones cristaloides y coloides para el shock han arrojado resultados contradictorios. En general, decida qué líquido administrar en función del estado del niño y de la respuesta a la reanimación inicial con una solución cristaloide isotónica.
Trás varios bolos de solución cristaloide isotónica, considere los coloides si
resulta indicado administrar más líquidos. Los coloides también pueden resultar
indicados en niños con un proceso
subyacente que puede estar asociado a una disminución de la presión oncótica del
plasma (p. ej.: desnutrición, hipoproteinemia, síndrome nefrótico).
Frecuencia y volumen
de administración de líquidos
Para
casos de shock, inicie la reanimación con líquidos con
un bolo de solución cristaloide isotónica de 20 ml/kg administrado entre 5 y 20
minutos. Repita con bolos de 20 ml/kg según sea necesario para restablecer la
perfusión presión arterial. A menudo es difícil precisar el volumen de déficit
de líquidos solo a partir de la historia del niño. Recurra a la
exploración física y a pruebas de laboratorio para identificar el volumen
necesario; puede que sea necesario administrar un déficit de volumen mayor del
estimado. Reevalúe con frecuencia.
Administre un bolo de líquidos más
rápido ante shock hipotenso y séptico. Por lo general, estos niños requieren al
menos 60 ml/kg de solución cristaloide isotónica durante la primera hora del
tratamiento; puede que sean necesarios 200 ml/kg ó más en las primeras 8 horas
del tratamiento.
Si se sospecha ó confirma un shock
obstructivo ó disfunción miocárdica, administre el líquido en menor voIumen o más
lentamente. Administre bolos de entre 5 y 10 ml/kg durante un periodo de 10 a 20
minutos y reevalúe frecuentemente para identificar signos de agravamiento del
estado respiratorio por edema pulmonar. Obtenga otras pruebas diagnósticas (p.
ej. ecocardiografía) y consulte a un experto para confirmar las sospechas y
saber cómo proceder. Prepárese para proporcionar ventilación asistida y el
manejo de la vía aérea con PEEP según sea necesario, si se desarrolla edema
pulmonar.
La modificación de la reanimación
con líquidos es apropiada en
niños con shock asociado a DKA, grandes quemaduras y algunas intoxicaciones
(particularmente las ocasionadas por sobredosis de bloqueadores de canales de
calcio y bloqueo beta-antiadrenérgico). Los niños con DKA podrían sufrir
deshidratación importante pero a menudo se encuentran en estado hiperosmolar
(debido a la hiperglucemia). La administración rápida de solución cristaloide y
la reducción de la osmolalidad sérica puede ser un factor de riesgo para el
edema cerebral. Los niños que han ingerido bloqueadores de canales de calcio o
bloqueos beta-antiadrenérgicos pueden tener disfunción miocárdica y ser menos
tolerantes a la expansión rápida del volumen.
La Tabla 4 sirve de guía general para los volúmenes y la frecuencia de
administración de bolos de líquidos en función de la causa subyacente del shock.

Administración rápida de líquidos
Los sistemas
de administración de líquidos IV de uso común para la administración de líquidos
en pediatría no administran los bolos de líquido tan rápidamente como lo
requiere el manejo de algunas formas de shock.
Para facilitar la administración rápida de líquidos :
Coloque un catéter IV lo más grande posible, especialmente si se necesita la administración de sangre o coloides
Coloque una llave de 3 vías en el sistema de sondas IV
Con una jeringa de 30 a 60 mi, inyecte el tíquido para que pase por la llave, o use una bolsa a presión (con atención a los riesgos de embolia aérea), o bien un dispositivo de infusión rápida
Nota: las bombas de infusión
estándar, incluso si se ajustan a la velocidad de infusión máxima, no
administran el líquido a la suficiente velocidad, especialmente en niños
mayores.
Por ejemplo, un paciente de 50 kg con shock séptico idóneamente debería recibir
1 I de solución cristaloide en un periodo de 5 a 10 minutos, en lugar de la hora
que tarda la bomba de infusión.
Reevaluación frecuente durante la reanimación con líquido
Las reevaluaciones frecuentes durante la reanimación con líquido son esenciales
para tratar el shock correctamente.
Esta reevaluación debe :
Valorar la respuesta fisiológica tras cada administración de bolo de líquidos
Determinar si es necesario administrar más bolos de líquidos
Valorar signos de efectos adversos (p. ej. edema pulmonar) durante y después de la reanimación con líquidos
Los signos de mejoría fisiológica incluyen una mejora en la perfusión, aumento
en la presión arterial, disminución de la frecuencia cardíaca (hacia un ritmo
normal), disminución de la frecuencia respiratoria (hacia un ritmo normal),
aumento de la diuresis y mejor estado mental. Si el estado del niño no mejora o
se agrava tras la administración de bolos de líquidos, intente identificar la
causa del shock para determinar las siguientes intervenciones. Por ejemplo, si
el llenado capilar sigue siendo prolongado a pesar de haberse administrado
líquidos inicialmente, podría estar señalando a una hemorragia continua u otra
pérdida de líquido. El deterioro del estado del niño tras la administración de
líquidos puede ser un signo de shock cardiogénico u obstructivo. Un aumento del
esfuerzo respiratorio podría indicar edema pulmonar.
Indicaciones para el uso de los
hemoderivados
Se recomiendan hemoderivados para compensar la pérdida de volumen traumática si
la perfusión del niño es inadecuada a pesar de la administración de 2 a 3 bolos
de 20 ml/kg de cristaloides isotónicos. En estas circunstancias, administre 10
ml/kg de concentrados de glóbulos rojos a la mayor brevedad.
Por lo general, en las emergencias no suele disponerse de sangre cuya
compatibilidad se haya determinado exactamente, ya que la mayoría de bancos
sanguíneos necesitan casi 1 hora para el proceso de pruebas cruzadas de
compatibilidad. Podría disponerse de sangre sometida a pruebas cruzadas en el
caso de niños estabilizados con solución cristaloide pero con pérdida de sangre
persistente. Las prioridades para el tipo de sangre o hemoderivados usados en
orden de preferencia son :
Sometida a pruebas cruzadas
Específica por grupo
Grupo O negativo (0- preferido para sexo femenino y 0+ u 0- para masculino)
Se puede usar sangre que no se haya sometido a pruebas cruzadas, específica del
grupo y Rh sanguíneo si la pérdida de sangre persistente provoca hipotensión a
pesar de la administración de solución cristaloide. La mayoría de bancos
sanguíneos necesitan 10 minutos para poder suministrar sangre de un grupo y Rh
sanguíneo específico. La sangre específica de un grupo y Rh sanguíneo tiene
idéntico tipo ASO y Rh, pero, a diferencia de la sangre con compatibilidad
confirmada mediante pruebas cruzadas, podrían darse incompatibilidades con otros
anticuerpos. Use el grupo y Rh sanguíneo O si es necesaria una transfusión
inmediata para evitar el paro cardiorrespiratorio, ya que se puede administrar a
niños con cualquier grupo y Rh sanguíneo. La sangre O negativo es preferible en
mujeres en edad de procrear para evitar la sensibilización al Rh. El grupo
sanguíneo O negativo o O positivo se puede administrar a los varones.
Complicaciones por la administración rápida de hemoderivados
La infusión rápida de sangre o hemoderivados fríos, particularmente en gran
volumen, puede producir complicaciones como :
Hipotermia
Disfunción miocárdica
Hipocalcemia ionizada
La hipotermia puede afectar a la función cardiovascular y a la coagulación y
comprometer diversas funciones metabólicas, como el metabolismo del citrato,
presente en la sangre almacenada. A su vez, una eliminación inadecuada de
citratos ocasiona hipocalcemia ionizada. Los efectos combinados de la hipotermia
y la hipocalcemia ionizada pueden ocasionar una disfunción miocárdica e
hipotensión importantes.
Para minimizar estos problemas, en lo posible, antes o durante la administración
rápida por vía IV, caliente la sangre y los hemoderivados con un dispositivo al
efecto aprobado para tal uso y disponible comercialmente. Prepare calcio por si
hubiera que administrarlo en caso de que el niño sufra de hipotensión durante la
transfusión rápida; en algunos casos, podría ser beneficioso administrar calcio
en la práctica para evitpr la hipocalcemia.
La experiencia en contextos bélicos recientes ha demostrado una mejora de la
supervivencia en pacientes con traumatismos que recibieron una transfusión
sanguínea (el volumen de sangre administrada supera el volumen de sangre del
paciente) cuando se transfunde el plasma con una relación aproximada de 1:1 a
los glóbulos rojos.
Glucosa
Vigile la concentración de glucosa en sangre como parte del manejo del shock. La
hipoglucemia es un signo común en niños con enfermedades graves. Puede ocasionar
lesión cerebral si no se identifica rápidamente y se trata con efectividad. En
un estudio pediátrico, la hipoglucemia estaba presente en el 18% de los niños
atendidos en un servicio de emergencias hospitalario por problemas relacionados
con disminución en el nivel de consciencia, estado epiléptico, insuficiencia
respiratoria, insuficiencia cardiopulmonar o paro cardíaco. Para obtener más
detalles consulte Losek, 2000 (la referencia completa se encuentra en la Lista
de lecturas recomendadas al final de este apartado).
|
Concepto crítico |
En los niños con enfermedades o lesiones graves, realice una prueba rápida de glucosa para descartar la hipoglucemia como causa o factor desencadenante del shock o menor nivel de consciencia. |
Control de la
glucosa
Mida la glucemia en los lactantes y niños con signos de disfunción neurológica
(p. ej.: convulsiones, coma), shock
o insuficiencia respiratoria. La glucemia se puede medir
con muestras de sangre arterial, venosa o capilar con una prueba rápida de
glucosa o mediante análisis de laboratorio. Los lactantes pequeños y niños con
enfermedad crónica tienen mayores niveles de utilización de glucosa y reservas
limitadas de glucógenos. Este suministro limitado se puede consumir rápidamente
durante episodios de esfuerzo fisiológico, dando lugar a la hipoglucemia. Los
lactantes que reciben líquidos por vía IV sin contenido en glucosa tienen más
riesgo de desarrollar hipoglucemia.
La hiperglucemia, también común en niños con enfermedades
o lesiones graves, puede producirse por una resistencia a la insulina inducida
por altos niveles de catecolaminas y cortisol endógenos. Aunque el control de la
concentración de glucosa en suero mediante la infusión de insulina mejoró los
resultados en estudios de pacientes adultos con enfermedades graves, no hay
datos suficientes que corroboren el uso rutinario de este tratamiento en niños
con enfermedades graves. En la medida de lo posible,
es preferible evitar la hiperglucemia. Considere tratar la hiperglucemia en
grupos de alto riesgo, como niños con lesión cerebral, sin dejar de controlar
atentamente la respuesta para evitar la hipoglucemia.
Diagnóstico de la
hipoglucemia
La hipoglucemia puede ser difícil de reconocer clínicamente
porque algunos niños podrían no presentar signos ni síntomas visibles (es decir,
hipoglucemia asintomática). En cambio, otros podrían mostrar signos clínicos
inespecíficos (p. ej.: perfusión deficiente, sudoración, taquicardia,
hipotermia, irritabilidad o somnolencia e hipotensión). Estos signos clínicos
también son comunes a muchas otras afecciones, incluida la hipoxemia, la
isquemia o el shock. Aunque no se aplican a todos los pacientes, los siguientes
valores de glucemia mínima aceptable pueden servir para definir la hipoglucemia :
| Edad | Definición consensuada de hipoglucemia |
| Neonatos prematuros y de término | < 45 mg/dl |
| Lactantes Niños Adolescentes | < 60 mg/dl |
El valor más bajo de glucosa normal suele proceder de muestras obtenidas en
niños y lactantes en ayunas y en reposo. Por tanto, puede ser difícil extrapolar
estos umbrales a la glucemia necesaria en un niño con enfermedades ó lesiones
graves y alterado.
Manejo de la
hipoglucemia
Si la glucemia es baja y el niño tiene síntomas mínimos y
el estado mental es normal, puede administrar glucosa por vía oral (p. ej.: zumo
de naranja u otro líquido con glucosa). Si la concentración es muy baja o el
niño está sintomático, debe administrar glucosa por vía IV con una dosis de
0,5 a 1 g/kg. La dextrosa por vía IV suele administrarse como solución glucosada
al 25% (2 a 4 ml/kg) o como
solución glucosada al 10% (5 a 10 ml/kg). La dextrosa es la misma sustancia que
la glucosa. Reevalúe la glucemia sérica tras la administración de dextrosa.
Administre una infusión continua de líquido con glucosa por vía IV para
evitar la hipoglucemia recurrente.
No inyecte líquidos con dextrosa para la reanimación con volumen del shock de
manera rutinaria. Puede causar hiperglucemia, un aumento de la osmolalidad sérica y diuresis osmótica, que agravará aún más la hipovolemia y el shock.
También puede desarrollarse un desequilibrio de electrolitos (p. ej.:
hiponatremia).
Manejo según
el tipo de
shock
El manejo efectivo del shock atiende a la etiología del
shock. Para el curso del proveedor de SVAP/PALS, el shock se clasifica en 4
tipos, según la causa subyacente. Sin embargo, este método de clasificación
obvia en exceso el estado fisiológico observado en los pacientes individuales.
Algunos niños con shock presentan síntomas de shock hipovolémico, distributivo y
cardiogénico, y desarrollan un tipo de
shock de forma más acusada. Un niño con shock grave puede desarrollar síntomas
de disfunción miocárdica y mala distribución del flujo sanguíneo. Para obtener
más información sobre la clasificación del shock según la etiología, consulte el
Apartado 6: "Reconocimiento del shock".
En esta sección, se describe el manejo de los siguientes tipos de shock :
Hipovolémico
Distributivo
Cardiogénico
Obstructivo
|
Concepto crítico
:
|
Es importante proporcionar una reanimación adecuada rápida con líquidos para tratar el shock hipovolémico. Evite los errores comunes de una administración de líquidos inadecuada o tardía en la secuencia de reanimación. |
Manejo del
shock hipovolémico
La reanimación con líquidos es el tratamiento principal para el shock
hipovolémico. Los niños con shock hipovolémico que reciben un volumen apropiado
de líquidos en la primera hora de la reanimación tienen más probabilidades de
supervivencia y recuperación. La administración puntual de líquidos es
fundamental para evitar que el shock hipovolémico compensado empeore a shock
hipotenso persistente.
Otros componentes para el manejo efectivo del shock hipovolémico son :
Identificar el tipo de pérdida de volumen (hemorrágico y no hemorrágico)
Compensar el déficit de volumen
Evitar y compensar las pérdidas continuadas (por ejemplo, hemorragia, diarrea continuada)
Restablecer el balance acidobásico
Corregir las alteraciones metabólicas
Determinación de la reanimación adecuada con líquidos
La reanimación adecuada con líquidos en el shock hipovolémico depende de lo siguiente :
Alcance de la depleción de volumen
Tipo de pérdida de volumen (p. ej.: sangre, líquido con electrolitos o líquido con proteínas y electrolitos)
El alcance de la depleción de volumen puede subestimarse y no tratarse adecuadamente. En muchos casos, la depleción de volumen se deriva de una ingesta inadecuada de líquidos. Los parámetros clínicos que ayudan a concluir el porcentaje de deshidratación incluyen :
Aspecto general
Presencia o ausencia de lágrimas y aspecto de los ojos (normales o hundidos)
Humedad de las mucosas
Elasticidad de la piel
Profundidad y frecuencia respiratoria
Frecuencia cardíaca
Presión arterial
Tiempo de llenado capilar
Diuresis
Estado mental
Por lo general, la deshidratación clínicamente significativa en niños se asocia a un descenso en volumen de al menos el 5% (esto es, 5% de pérdida de peso corporal) lo que equivale a un déficit de líquidos de 50 mI/kg. Por tanto, quizá sea insuficiente tratar a un niño con deshidratación clínicamente evidente con un solo bolo de solución cristaloide isotónica de 20 mI/kg. Sin embargo, no suele ser necesario corregir completamente el déficit estimado en la primera hora. Tras restablecerse la perfusión, y si el niño ya no está en shock, el déficit total de líquidos podría ir corrigiéndose en las siguientes 24 a 48 horas.
Aunque todas las formas de shock hipovolémico se tratan inicialmente con
infusión rápida de solución cristaloide isotónica, la identificación rápida del
tipo de pérdida de volumen puede optimizar el tratamiento aún más. Las pérdidas
de líquidos se pueden clasificar como hemorrágicas y no hemorrágicas. Entre las
pérdidas no hemorrágicas se incluyen los líquidos que contienen electrolitos
(por ejemplo, diarrea, vómitos, diuresis osmótica asociada a DKA) y líquidos que
contienen proteínas y electrolitos (por ejemplo, pérdidas asociadas a quemaduras
y peritonitis).
Shock hipovolémico no hemorrágico
La pérdida de líquido no hemorrágico suele tener origen
gastrointestinal (vómitos y diarrea), urinario (DKA) y capilar (quemaduras). La
hipovolemia causada por pérdida de líquido no hemorrágico suele clasificarse en
términos
de porcentaje de pérdida de peso corporal (Tabla 5). La correlación entre
presión arterial y déficit de líquido es imprecisa. Sin embargo, como regla
general el shock hipotenso se puede observar en niños con déficits de líquidos
de 50 a 100 ml/kg, pero es más evidente cuando el déficit es ≥
100 ml
/ kg.
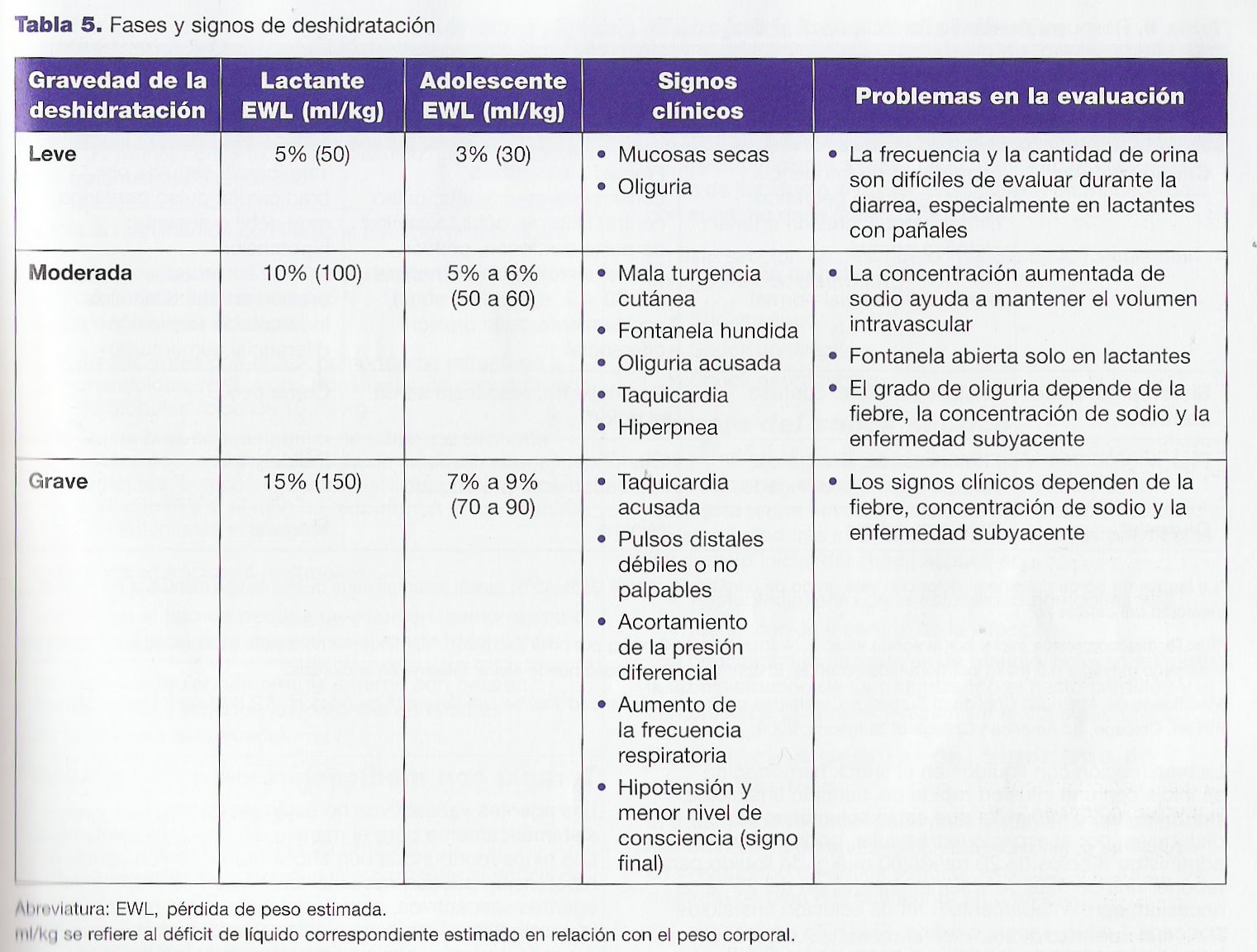
Tratamiento
Administre soluciones cristaloides isotónicas en volumen de 20 ml/kg para tratar con eficacia a un niño con shock hipovolémico asociado a la deshidratación. Si no mejora después de haber administrado al menos 3 bolos (es decir, 60 ml/kg) cabe pensar lo siguiente :
El alcance de la pérdida de líquido se ha subestimado
El tipo de líquido debe cambiarse (p. ej.: hay que administrar coloides o sangre)
Hay pérdida constante de líquido (p. ej.: hemorragia oculta)
Su idea inicial sobre la etiología del shock puede ser errónea (esto es, considere una alternativa ó tipos de shock combinados)
Las pérdidas constantes de líquido (p. ej.: diarrea,
DKA,
quemaduras) deben reponerse además de corregirse los déficits existentes. El
coloide no está indicado
sistemáticamente como tratamiento inicial del shock hipovolémico. Sin embargo,
la albúmina y otros coloides se han usado con éxito para la reposición de
volumen en niños con pérdidas importantes del "tercer espacio"
ó déficits de albúmina.
|
Concepto crítico
:
|
Para la reanimación con líquidos del shock hemorrágico, administre unos 3 ml de solución cristaloide por cada 1 ml de sangre perdida. |
Shock hipovolémico hemorrágico
El shock hipovolémico hemorrágico se clasifica según un porcentaje estimado de pérdida de volumen sanguíneo total (Tabla 6). En niños, la línea divisoria entre shock hemorrágico compensado leve y moderado frente a moderado o grave y shock hemorrágico hipotenso se corresponde con una pérdida aproximada de volumen sanguíneo del 30%. En niños, se calcula un volumen sanguíneo total de 75 a 80 ml/kg; por tanto, una pérdida del 30% representa una pérdida sanguínea de aproximadamente 25 mI/kg.
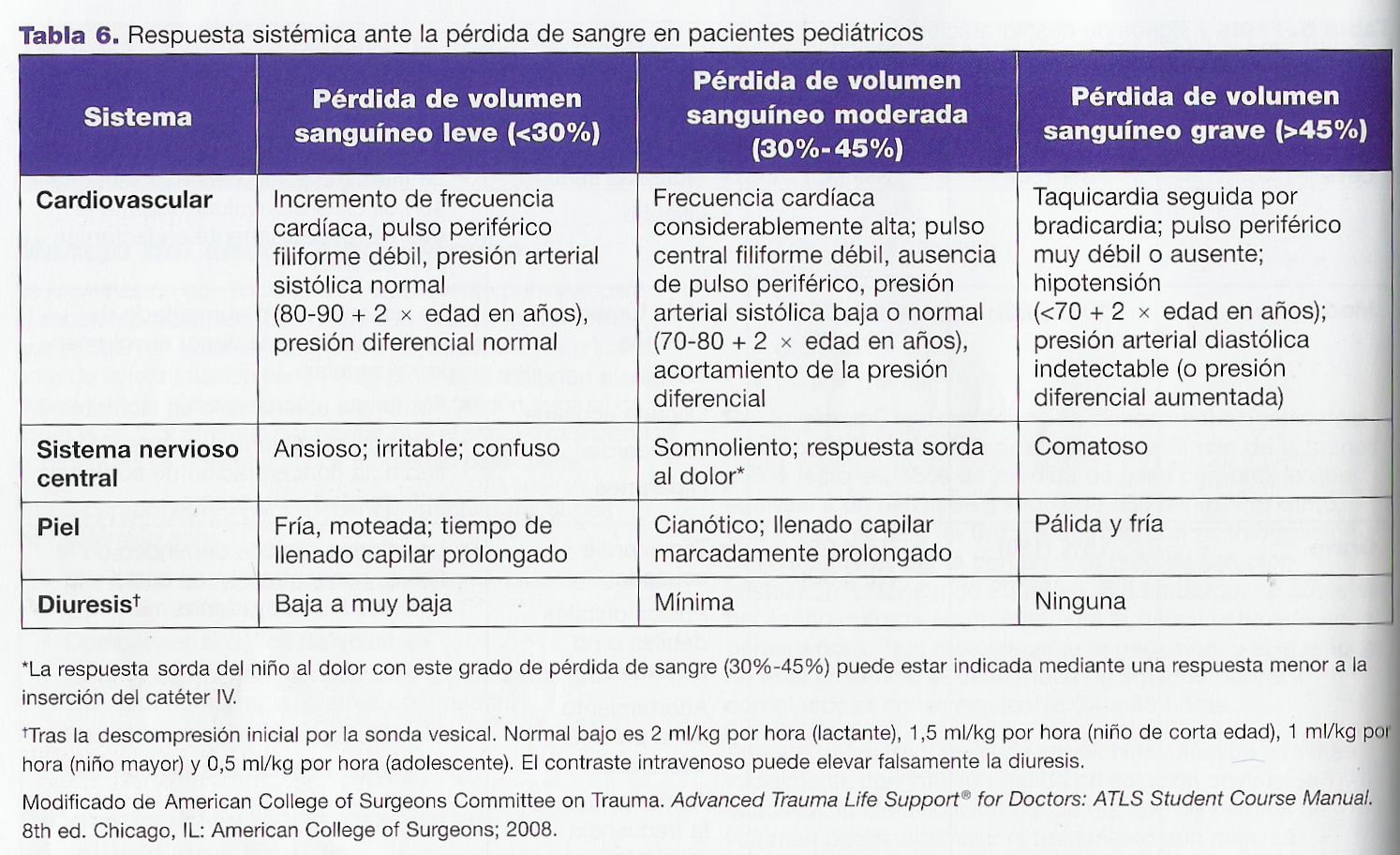
La reanimación con líquidos en el shock hemorrágico
se inicia con una infusión rápida de solución cristaloide isotónica de 20 mI/kg.
Ya que estas soluciones se distribuyen por el espacio extracelular, podría ser
necesario administrar 3 bolos de 20 ml/kg (60 ml/kg) de líquido para reponer una
pérdida de volumen sanguíneo del 25%; se necesitan aproximadamente 3 mi de
solución cristaloide por cada 1 mi de sangre perdida. Si el niño permanece
hemodinámicamente inestable a pesar de los 2 ó 3
bolos de cristaloide isotónico de 20 ml/kg, considere una transfusión de
concentrados de glóbulos rojos.
Para la reposición de sangre, use concentrados de glóbulos rojos de 10 ml/kg. Se
puede administrar sangre completa (20 ml/kg) en lugar de concentrados de
glóbulos rojos, pero es más difícil y se tarda más tiempo en obtener. Además, el
riesgo de reacciones a la transfusión aumenta considerablemente si la sangre no
se ha sometido a pruebas cruzadas. Para minimizar los efectos adversos, caliente
la sangre en un dispositivo al efecto si hay alguno disponible, especialmente
cuando transfunda rápidaménte.
La transfusión para el shock hemorrágico está indicada cuando hay :
Perfusión deficiente o hipotensión refractaria a cristaloides
Pérdida considerable de sangre
El shock hemorrágico refractario a cristaloides se
define como hipotensión persistente a pesar de administrarse soluciones
cristaloides en volumen de 40 a 60 ml/kg. Los niños con hemorragia rápida pueden
mostrar una concentración de hemoglobina inicial normal o baja. Transfunda
sangre en caso de una concentracion de hemoglobina baja porque la anemia aumenta
el riesgo de hipoxia tisular debido a un contenido y aporte de O2 inadecuados.
Terapia con medicación
Los agentes vasoactivos no están indicados
sistemáticamente para el manejo del shock hipovolémico. Los niños moribundos con
shock hipovolémico agudo e hipotensión pueden necesitar administración rápida de
agentes vasoactivos, como adrenalina, para restablecer la contractilidad
cardíaca y el tono vascular hasta que se proceda con una reanimación adecuada
con líquidos.
Balance acidobásico
En las primeras fases de la progresión de shock hipovolémico, el niño puede
desarrollar taquiapnea y alcalosis respiratoria. Sin embargo, la alcalosis no
corrige completamente la acidosis (Iáctica) metabólica derivada del shock
hipovolémico. Un niño con shock persistente o grave puede padecer una acidosis
grave porque el niño termina desarrollando fatiga o insuficiencia
cardiorrespiratoria. Los niños con lesiones torácicas o craneoencefálicas
podrían no mostrar taquiapnea compensatoria.
La acidosis persistente y la perfusión deficiente son indicativos de que la
reanimación no es adecuada o, en casos de shock hemorrágico, de una pérdida
continua de sangre. No se recomienda el bicarbonato sódico para tratar la
acidosis metabólica asociada al shock hipovolémico. Si la reanimación con
líquidos mejora la perfusión y la función de los órganos vitales, la acidosis
metabólica se tolera bien y se corrige gradualmente.
El
bicarbonato
está indicado si la acidosis metabólica se debe a pérdidas importantes de
bicarbonato con origen renal o gastrointestinal (es decir, una acidosis
metabólica sin anión gap), porque es difícil compensar una pérdida constante de
bicarbonato.
Consideraciones específicas de tratamiento
Siga los principios de manejo inicial (Tabla 3) además de las siguientes consideraciones específicas para el shock hipovolémico que se muestra en la Tabla 7 :

Manejo del shock distributivo
El manejo inicial del shock distributivo se centra en aumentar el volumen intravascular para corregir la hipovolemia y llenar el espacio
vascular aumentado dilatado. Use agentes vasoactivos si el niño permanece
hipotenso o con una perfusión deficiente a pesar de la administración rápida de
bolos de líquidos o si la presión diastólica permanece baja con aumento de la
presión diferencial.
En esta sección se describe el manejo de los siguientes tipos de shock distributivo :
Shock séptico
Shock anafiláctico
Shock neurogénico
Manejo del shock séptico
Los cambios clínicos, hemodinámicos y metabólicos observados en el shock séptico
son resultado de la respuesta a una infección, incluida la liberación o
activación de los mediadores inflamatorios.
Los objetivos principales del manejo inicial del shock séptico son :
Restablecimiento de la estabilidad hemodinámica
Identificación y control de la infección
Los principios fundamentales de manejo incluyen aumentar la administración de O2
optimizando el gasto cardíaco y el contenido de O2 arterial y minimizar el
consumo de O2,
Descripción general del algoritmo
shock séptico
El
tratamiento
recomendado para restablecer la estabilidad hemodinámica para el shock séptico
en niños se incluye en el algoritmo de shock séptico pediátrico (Figura 1). Se
describe un plan de tratamiento en 3 niveles :
Administrar O2, asistir la ventilación, controlar la frecuencia respiratoria, la saturación de O2, la frecuencia cardíaca, la presión arterial y la temperatu~ y determinar el acceso vascular.
Iniciar la administración intensiva de bolos de líquidos isotónicos durante la primera hora con reevaluaciones frecuentes de perfusión y monitorizar signos de edema pulmonar o hepatomegalia.
Tratar el shock séptico refractario a líquidos con agentes vasoactivos.
Anticiparse a la insuficiencia adrenal y administrar dosis de estrés de hidrocortisona si el niño no responde a la medicación vasoactiva.
Shock séptico
|
Identificar e intervenir : Shock séptico |
La identificación rápida del shock séptico es crucial para iniciar la reanimación y evitar el paro cardíaco. El soporte hemodinámico para mantener el suministro de O2 puede reducir la morbimortalidad pediátrica de shock séptico. |
Figura 1.- Algoritmo de shock séptico
pediátrico
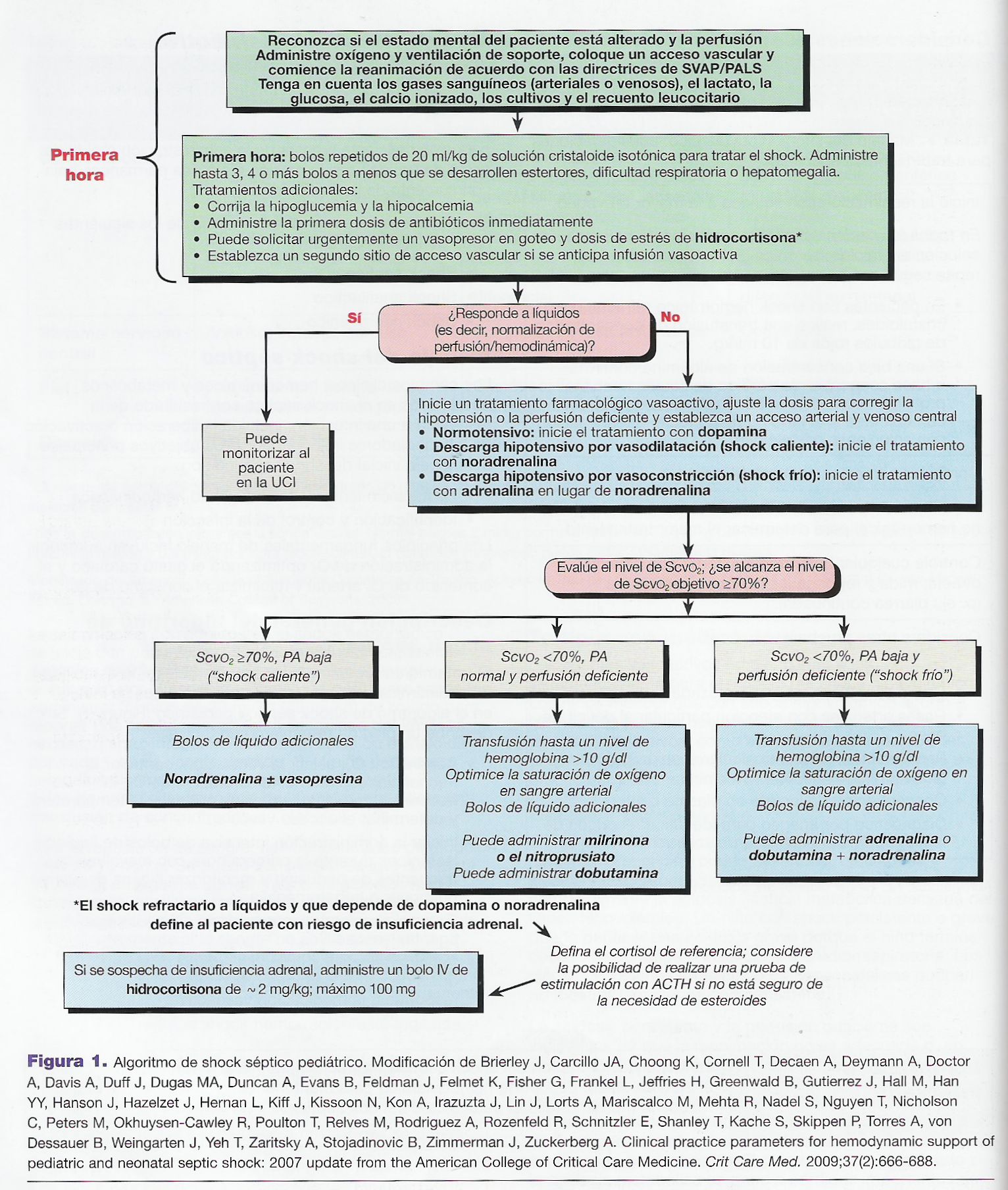
El tratamiento adecuado durante la primera hora es decisivo para maximizar las posibilidades de supervivencia en niños con shock séptico. La intubación y ventilación mecánica tempranas podrían estar indicadas en caso de disminución del nivel de consciencia o para reducir el esfuerzo respiratorio. Los componentes iniciales del manejo del shock séptico son :
Administración rápida e intensiva de bolos de líquidos
Administración rápida de antibióticos tras la obtención de cultivos, si es posible
Inicio rápido del soporte hemodinámico, incluidos vasopresores y dosis de estrés de hidrocortisona
Identificación y corrección de las alteraciones metabólicas
Pruebas diagnósticas (p. ej.: concentración de lactato, déficit de base y saturación de O2 venoso central) para identificar la gravedad del shock y controlar la respuesta a la administración de líquidos
La administración rápida e intensiva de líquidos es una prioridad. Un volumen intravascular inadecuado provoca un bajo volumen sistólico e hipotensión.
Un
niño con shock séptico suele necesitar un gran volumen de líquido para
restablecer la perfusión. Administre rápidamente 3
ó 4 bolos (20 ml/kg
cada
uno) de solución cristaloide isotónica. Dosifique
el volumen y la frecuencia de la administración de líquidos evaluando
continuamente los siguientes parámetros: perfusión tisular, frecuencia cardíaca,
presencia y calidad de los pulsos periféricos, llenado capilar, temperatura de
la piel, nivel de consciencia y diuresis.
El edema pulmonar podría desarrollarse durante la administración de líquidos,
pero realmente es más probable que aparezca si la administración de líquidos no
es adecuada. Por lo general, los líquidos se deben administrar rápidamente aun
cuando aumente la permeabilidad capilar y el riesgo de edema pulmonar. Si el
edema pulmonar
es cardiogénico (hepatomegalia, cardiomegalia, mala contractilidad miocárdica),
quizá deba reducir el volumen y la frecuencia de la administración de líquidos.
Si se desarrolla un edema pulmonar no cardiogénico importante, el niño podría
necesitar la inserción de un dispositivo avanzado para la vía aérea
y
ventilación
asistida mecánica con O2 adicional y PEEP.
Tome muestras sanguíneas para cultivo. Administre la primera dosis de
antibióticos de amplio espectro a la mayor brevedad. En casos de sepsis, no
retrase el tratamiento antimicrobiano a la espera de los cultivos sanguíneos ni
para realizar otras pruebas diagnósticas, como una punción lumbar. Cuando sea
posible, obtenga también muestras de sangre venosa central o arterial, o ambas,
para gasometría y medición de la concentración de lactato. La comparación entre
saturación de O2 venoso central y saturación de O2
arterial puede ofrecer una estimación del gasto cardíaco.
Prevea que quizá deba administrar vasopresores y dosis de estrés de
hidrocortisona. Solicite previamente estos fármacos a la farmacia para que se
puedan administrar al instante. Deben estar disponibles de inmediato si el niño
no responde al tratamiento con líquidos o se sospecha de una insuficiencia
adrenal.
Identifique y corrija las alteraciones metabólicas de inmediato.
La hipoglucemia y la hipocalcemia ionizada son comunes en el shock séptico y
pueden propiciar la disfunción miocárdica.
Use las pruebas diagnósticas (p. ej.: concentración de lactato, déficit de base
y saturación de O2 venoso central) para identificar la gravedad del shock y
controlar la respuesta a la administración de líquidos.
Tras el tratamiento inicial, evalúe la frecuencia cardíaca, la presión arterial
y la perfusión periférica para determinar la siguiente intervención. Si la
frecuencia cardíaca, la presión arterial y la perfusión están volviendo a los
valores normales, prepare el ingreso o traslado a un centro pediátrico adecuado.
Si el niño permanece hipotenso o con mala perfusión, continúe con el siguiente
nivel del algoritmo. Consulte con una unidad de cuidados intensivos pediátrica o
con el equipo encargado del traslado. Continúe con la reanimación mientras
prepara el ingreso o el traslado.
Tratamiento del
shock séptico
resistente
a líquidos
Si el shock grave continúa a pesar de una administración rápida e intensiva de
solución cristaloide isotónica durante la primera hora, inicie el tratamiento
para el shock séptico refractario a líquidos :
Establezca un acceso venoso central y arterial si no se hizo anteriormente.
Administre vasoactivos para mejorar la perfusión tisular y la presión arterial.
Administre más bolos de 20 ml/kg de solución cristaloide isotónica y considere inyectar un líquido con coloides.
Si la concentración de hemoglobina es <10 g/dl, considere la transfusión para aumentar la capacidad de transporte de O2,
Considere una ventilación asistida con O2 adicional y PEEP rápida, según sea necesario.
El tratamiento con medicación dependerá de la presión arterial (incluida la
presión diferencial), la evaluación de
la resistencia vascular (incluidos los pulsos periféricos, la temperatura y la
perfusión) y la SCVO2' si es posible. Con la exploración física no siempre se
obtienen evidencias claras de vasodilatación o vasoconstricción. Por ejemplo,
algunos niños con extremidades frías pueden tener vasodilatación pero perfusión
deficiente debido a un bajo volumen sistólico y una función cardíaca deficiente.
Las razones para optar por un fármaco u otro según el tipo de shock se
describen a continuación.
Shock "caliente"
La noradrenalina es
el agente vasoactivo de elección
para niños con shock séptico refractario a líquidos que presentan un shock
vasodilatado ("caliente") con perfusión deficiente o hipotensión. La
noradrenalina está indicada por sus potentes efectos vasoconstrictores
alfa-adrenérgicos, que pueden aumentar la presión arterial diastólica
incrementando la RVS. Asimismo, resulta indicada por su capacidad para aumentar
la contractilidad cardíaca con apenas cambios en la frecuencia cardíaca. Puede
restablecer la presión arterial aumentando la RVS, el tono venoso y el volumen
sistólico.
Una infusión de vasopresina puede
ser útil en caso de
shock refractario a noradrenalina. La vasopresina
antagoniza los mecanismos de la vasodilatación por sepsis. Actúa en conjunto con
las catecolaminas endógenas y exógenas para la estabilización de la presión
arterial, pero no afecta a la contractilidad cardíaca.
Shock normotenso
La dopamina es el agente vasoactivo más indicado para niños con shock séptico
refractario a líquidos, que presentan perfusión deficiente pero una presión
arterial adecuada. Según la dosis, la dopamina tiene diversos efectos. A dosis
bajas, la dopamina mejora el flujo sanguíneo renal y esplácnico. A dosis
intermedias, mejora la contractilidad cardíaca. A dosis elevadas, aumenta la RVS.
Si la perfusión del niño no mejora rápidamente con una infusión de dopamina,
inicie la infusión de adrenalina o noradrenalina. Según la presión diferencial y
la exploración física del niño, use adrenalina si la resistencia vascular es
normal o alta; use noradrenalina si la resistencia vascular es baja.
Los vasodilatadores pueden ayudar a mejorar la perfusión tisular en niños
normotensos con RVS alta, a pesar de la reanimación con líquidos y el inicio de
tratamientos para la contractilidad.
Si la mala perfusión continúa a pesar de la dopamina, considere añadir milrinona
o nitroprusiato al tratamiento. La milrinona es un inhibidor de la
fosfodiesterasa que tiene efectos vasodilatadores e inotrópicos. El
nitroprusiato es un vasodilatador puro.
También puede considerar la dobutamina. La dobutamina tiene efectos inotrópicos
y vasodilatadores, pero a menudo causa taquicardia y puede reducir sustancialmente la RVS con la consiguiente hipotensión.
Shock "frío"
La adrenalina es el agente vasoactivo más indicado para tratar el shock "frío".
Tiene potentes efectos inotrópicos que mejoran el volumen sistólico. La dosis de
adrenalina se puede ajustar para asistir la presión arterial y la mala
perfusión. En dosis de infusión bajas, la adrenalina puede reducir la RVS (por
sus efectos beta-adrenérgicos). En dosis de infusión altas, la adrenalina puede
aumentar la RVS (por su acción alfa-adrenérgica).
Una dosis de infusión de
adrenalina a una proporción de
≥
0,3
mcg/kg
por minuto
suele producir una acción alfa-adrenérgica. La adrenalina puede
aumentar los niveles de lactato mediante la estimulación de la producción de
lactato en el músculo esquelético.
También cabe considerar una combinación de dobutamina y noradrenalina, dada su
eficacia en adultos con shock séptico. La infusión de noradrenalina compensa la
tendencia de la dobutamina a causar una reducción excesiva de la RVS y
restablece mejor la perfusión esplácnica.
Corrección de la insuficiencia adrenal
Un
niño con shock séptico refractario a la reposición de volumen y
dependiente de la dopamina o la noradrenalina puede desarrollar
insuficiencia adrenal. Si es
posible, determine el nivel inicial de cortisol. Si no hay datos prospectivos
para definir la insuficiencia adrenal en función del nivel de cortisol, la
insuficiencia adrenal puede estar presente si el nivel aleatorio de cortisol es
<18 mcg/dl (496 nmol/I).
Si se sospecha o confirma la insuficiencia adrenal, administre un bolo de
hidrocortisona de 2 mg/kg por vía IV (dosis máxima 100 mg).
|
Dato
fundamental : |
Si el diagnóstico de la insuficiencia adrenal no es claro, confirme con una prueba de estimulación con corticotropinas. Un aumento en los niveles de cortisol de ≤ 9 mcg/dl (248 nmol/I) tras una prueba de estimulación con corticotropinas de 30 ó 60 minutos es suficiente para confirmar el diagnóstico de insuficiencia adrenal. |
Criterios de
valoración terapéutica
Dosifique los agentes vaso activos en el shock séptico de acuerdo a los criterios de valoración terapéutica, como :
Perfusión y pulsos distales buenos
Presión arterial adecuada
SCVO2 ≥ 70%
Mejora de la acidosis metabólica y la concentración de lactato
Se recomienda la observación estricta de los criterios de evaluación para evitar
una vasoconstricción excesiva en ICE órganos vitales.
Manejo del shock anafilácfico
El manejo del shock anafiláctico se centra en corregir
los problemas cardiopulmonares que amenazan la vida
y en anular o bloquear los mediadores liberados como parte de una respuesta
alérgica no controlada. Ya que el angioedema (tumefacción tisular por un aumento
acusado de la permeabilidad capilar) puede provocar la obstrucciór total de la
vía aérea superior, los profesionales deben anticiparse a la necesidad de
intervención rápida de la vía aérea con ventilación asistida. El tratamiento
principal es la administración de adrenalina para revertir la hipotensiór y la
liberación de histamina y otros mediadores alérgicos. La reanimación con
líquidos también podría contribuir al restablecimiento de la presión arterial.
Consideraciones específicas
de tratamiento
Considere el manejo inicial general del shock descrito en la
Tabla 3 además
de los siguientes tratamientos específicos '"lndicados para el shock anafiláctico
(Tabla 8).
Tabla 8. Manejo
del shock anafiláctico: consideraciones para tratamientos específicos
Adrenalina
La administración de adrenalina por vía 1M (1:1000) o de adrenalina con un autoinyector (pediátrico o adulto, en función de la talla del niño) es el elemento más importante para el tratamiento de la anafilaxia.
Puede que sea necesaria una segunda dosis ó una infusión de adrenalina transcurridos de 10 a 15 minutos en casos de anafilaxia grave.
Administre bolos de líquido cristaloide isotónico según sea necesario para asistir a la circulación.
Salbutamol
Administre salbutamol en caso necesario para tratar el broncoespasmo mediante un inhalador de dosis medida, un nebulizador continuo o uno intermitente.
Antihistamínicos
Antihistamínico H1 (difenhidramina).
Considere un antihistamínico H2 (esto es, ranitidina o famotidina).
Nota: administrar los antihistamínicos H1 y H2 combinados puede ser más efectivo que administrar solo uno de ellos.
Corticosteroides
Metilprednisolona o corticosteroide equivalente
Para hipotensión refractaria a la adrenalina por vía 1M y a líq~dos, use vasopresores según lo indicado.
Infusión de adrenalina (1:10 000); dosifique según sea necesario. Las dosis frecuentes bajas < 0,05 mcg/kg por minuto) son eficaces.
Siga observando para identificar y tratar síntomas tardíos. Entre el 25% y 30%
de los niños podrían presentar síntomas tardíos varias horas después de los
síntomas agudos observados originalmente. La probabilidad de que se presenten
síntomas tardíos aumenta proporcionalmente. oon la gravedad de los síntomas
agudos.
Manejo del shock neurogénico
Los
niños con shock neurogénico suelen presentar
hipotensión, bradicardia y algunas veces hipotermia.
Se suele observar una respuesta mínima a la reanimación con líquidos. La presión
arterial se caracteriza por una baja presión arterial diastólica con aumento de
la presión diferencial por la pérdida de tono vascular. Los niños con shock
medular pueden ser más sensibles a las variaciones de la temperatura ambiente y
podrían necesitar enfriarse o calentarse.
Consideraciones específicas de tratamiento
Podrían aplicarse los principios de manejo inicial para el shock descritos en la
Tabla 3 además de los siguientes tratamientos específicos para el shock
neurogénico según resulten indicados (Tabla
9).
Tabla 9. Manejo
del shock neurogénico: consideraciones para
tratamientos específicos
Coloque al paciente en una posicion tumbado ó con la cabeza hacia abajo para mejorar el retorno venoso.
Priuebe con la administración de líquidos (solución cristaloide isotónica ) y valore la respuesta
Para la hipotensión refractaria a liquidos, utilice vasopresores (p. ej., adrenalina [epinefrina], noradrenalina [norepinefrina]), segun lo indicado.
Enfríe ó caliente al paciente segun sea necesario.
Manejo del shock cardiogénico
El shock cardiogénico es una alteración por una perfusión
tisular inadecuada resultado de una disfunción miocárdica. Inicialmente, el
shock cardiogénico podría parecer shock hipovolémico, por lo que identificar la
etiología cardiogénica puede resultar difícil. Si sospecha de shock cardiogénico,
considere probar con una administración lenta (de 10 a
20 minutos) de bolo de líquidos (bolo de 5 a 10 ml/kg) mientras supervisa
atentamente la respuesta del niño.
Es probable que exista shock cardiogénico si el niño no mejora, la función
respiratoria empeora o se desarrollan signos de edema pulmonar. La evidencia de
congestión venosa (p. ej.: ingurgitación yugular o hepatomegalia) y
cardiomegalia (en la radiografía de tórax) también sugieren un shock de
etiología cardíaca.
Objetivos principales
Un objetivo principal en el manejo del shock carcjiogénico
es mejorar la eficacia de la función cardíaca y el gasto cardíaco optimizando la
eyección ventricular. Otro objetivo principal es minimizar el requerimiento
metabólico. Muchos niños con shock cardiogénico tienen una precarga alta y no
requieren administración de líquidos adicional. En otros podría ser necesario
administrar con cautela un bolo de líquidos para aumentar la precarga. La forma
más efectiva de aumentar el volumen sistólico es reducir la poscarga (RVS) en
lugar de administrar un agente inotrópico. Los inotrópicos pueden aumentar
la contractilidad cardíaca, pero también aumentan la demanda de O2 miocárdico.
Sin embargo, los niños que ya están hipotensos pueden necesitar la
administración de líquidos e inotrópicos para tolerar la reducción de la
poscarga.
El manejo específico incluye :
Administración cautelosa de líquidos y monitorización
Pruebas de laboratorio y otras pruebas diagnósticas
Medicaciones
Asistencia circulatoria mecánica
Consulte a la unidad de cuidados intensivos pediátrica o un especialista en
cardiología pediátrica lo antes posible. Ayudará a facilitar un diagnóstico (p.
ej.: ecocardiografía), orientar las siguientes intervenciones y organizar el
traslado para la atención definitiva.
Administración cautelosa de líquidos y monitorización
Un corazón de gran tamaño en una radiografía de tórax en un niño con evidencia
de shock y escaso gasto cardíaco es distintivo de shock cardiogénico con volumen
intravascular adecuado. Obtenga una ecocardiografía para disponer
de datos más objetivos y precisos sobre la precarga
y función cardíaca. Si los datos objetivos o la historia
del niño (p. ej.: vómito y mala ingestión) son propios de una precarga
inadecuada, debe administrar un bolo de líquidos con
cautela (de 5 a 10 ml/kg de 10 a
20 minutos). Valore la función respiratoria frecuentemente durante la
administración de líquidos. Vigile por si se desarrolla edema pulmonar y empeora
la función pulmonar. Administre O2 adicional. Prepárese para ofrecer ventilación
asistida.
La presión positiva no invasiva podría descartar la ventilación
mecánica si se reduce el esfuerzo respiratorio y mejora la oxigenación.
Considere establecer un acceso venoso central para facilitar la medición de la
presión venosa central con el fin de disponer de un valor de referencia del
estado de precarga y poder realizar varias infusiones. Además, el acceso venoso
central permite monitorizar la saturación de O2 venoso central como medición
objetiva de la idoneidad de la administración de O2 en función del requerimiento
metabólico. La monitorización invasiva con catéter arterial pulmonar, una opción
en la unidad de cuidados intensivos pediátrica, no es decisiva para el
diagnóstico del shock cardiogénico. Sin embargo, en algunos casos un catéter de
arteria pulmonar puede ayudar a orientar la reanimación con líquidos y las
infusiones vasoactivas, particularmente si es necesario evaluar la precarga del
ventrículo izquierc]().
Pruebas de laboratorio y otras pruebas diagnósticas
Obtenga
pruebas
de laboratorio para evaluar el impacto del shock
en la función de los órganos vitales. Ninguna prueba de laboratorio es
totalmente sensible o específica para el shock cardiogénico. Las pruebas
apropiadas a menudo incluyen :
Gases arteriales para determinar la magnitud de la acidosis metabólica y la idoneidad de la oxigenación y ventilación
Concentración de hemoglobina para confirmar que la capacidad de transporte de O2 es adecuada
Concentración de lactato y saturación de O2 venoso central como indicadores de la idoneidad de la administración de O2 en función del requerimiento metabólico
Pruebas de la función tiroidea y enzimas cardíacas
Otras pruebas útiles incluyen:
|
Prueba |
Uso |
|
Radiografía de tórax |
Ofrece información sobre el tamaño del corazón, marcas vasculares pulmonares, edema pulmonar y patología pulmonar coexistente . |
|
ECG |
Puede detectar arritmia, característica de lesión miocárdica, cardiopatía isquémica o evidencia de intoxicación por fármacos |
|
Ecocardiografía |
Puede ser una prueba diagnóstica para revelar una cardiopatía congénita, movimiento de la paree ventricular acinético o discinético ó disfunción valvular; también ofrece una medición objetiva de la función y volumen de la cavidad ventricular (precarga). |
Medicaciones
Si el niño está normotenso, el tratamiento con medicaciones
consiste en diuréticos y vasodilatadores. Los diuréticos están indicados en
niños con evidencia de edema pulmonar ó congestión venosa sistémica. Los
vasodilatadores suelen administrarse por infusión continua.
Los niños con shock cardiogénico podrían necesitar medicación para aumentar el
gasto cardíaco mejorando
la contractilidad. La mayoría también necesita agentes para reducir la
resistencia vascular periférica. Se incluyen vasodilatadores, inotrópicos e
inhibidores de la enzima fosfodiesterasa (inodilatadores). La milrinona es el
fármaco más usado en muchos centros. Para obtener información detallada de estos
fármacos, consulte "Terapia con medicación" en la sección "Manejo general del
shock" en este apartado.
Un aumento del requerimiento metabólico, particularmente una mayor demanda de O2
miocárdico, contribuye al ciclo progresivo del shock cardiogénico. Reducir el
requerimiento metabólico es un componente fundamental en el manejo del shock
cardiogénico. Recurra a la ventilación asistida y a los antipiréticos para
reducir el requerimiento metabólico. Los analgésicos y sedantes reducen el
consumo de O2, pero también la respuesta endógena al esfuerzo. Administre, estos
agentes en dosis pequeñas. Supervise al niño para detectar signos de una posible
hipotensión o deprésión respiratoria.
Asistencia circulatoria mecánica
Los niños con shock cardiogénico que no responden
al tratamiento médico pueden beneficiarse de una asistencia circulatoria
mecánica si la causa del shock puede ser reversible. Un soporte vital
extracorpóreo puede mantener temporalmente el gasto cardíaco, la oxigenación y
ventilación mientras se trata la causa subyacente de insuficiencia
cardiopulmonar.
Las formas de soporte vital extracorpóreo incluyen oxigenación
de la membrana extracorpórea y dispositivos para asistir a
la función ventricular. El soporte vital extracorpóreo suele estar disponible en
centros pediátricos especializados con los recursos y la experiencia para tratar
a niños con insuficiencia cardiopulmonar aguda.
Consideraciones específicas de tratamiento
Siga los principios de manejo inicial para el shock descritos en la Tabla 3 además de las siguientes consideraciones específicas para el shock cardiogénico (Tabla 10).
Tabla 10.
Manejo del shock cardiogénico: consideraciones para el tratamiento específico
Administre un bolo de solución cristaloide isotónica de entre 5 a 10 ml/kg (entre 10 a 20 minutos), repita segun sea necesario.
Administre oxigeno suplementario y considere si es necesaria la presión positiva no invasiva ó la ventilacion mecanica.
Evalue frecuentemente si hay edema pulmonar.
Considere la aistencia circulatoria mecánica.
Manejo del
shock obstructivo
El manejo del shock obstructivo es específico del tipo de
obstrucción. En esta sección se describe el manejo de :
Taponamiento cardíaco
Neumotórax a tensión
Lesiones cardíacas congénitas ductus-dependientes
Embolia pulmonar masiva
Objetivos principales
La presentación clínica temprana del shock obstructivo
puede ser similar al shock hipovolémico. Un enfoque de tratamiento inicial
razonable puede incluir probar con la administración de líquidos (solución
cristaloide isotónica en volumen de 10 a 20 ml/kg). La identificación rápida
del shock obstructivo con la evaluación secundaria y las pruebas diagnósticas es
decisiva para la efectividad del tratamiento.
Los principales objetivos del manejo del shock obstructivo son :
Corregir la causa de la obstrucción del gasto cardíaco
Restablecer la perfusión tisular
Principios generales de manejo
Además de las consideraciones específicas para la etiología de la obstrucción,
siga los principios del manejo inicial descritos en la sección "Aspectos básicos
del manejo del shock".
Manejo específico del taponamiento cardíaco
El
taponamiento cardíaco está ocasionado por la acumulación de líquidos, sangre o
aire en el espacio pericárdico. Esta acumulación limita el retorno venoso
sistémico, afecta al llenado ventricular y reduce el gasto cardíaco. El
resultado favorable requiere la inmediatez
de la identificación y del tratamiento. Los niños con taponamiento cardíaco
pueden mejorar temporalmente con la administración de líquidos que aumenten el
gasto cardíaco y la perfusión tisular hasta que se pueda realizar el drenaje
pericárdico.
Consulte a los especialistas apropiados (unidad de cuidados intensivos
pediátrica, cardiología pediátrica, cirugía pediátrica). El drenaje pericárdico
optativo (pericardiocentesis) a menudo orientado por ecocardiografía o
radioscopia, deberán realizarlo especialistas capacitados y formados en este
procedimiento. La pericardiocentesis de emergencia puede realizarse en caso de
paro cardíaco existente o inminente cuando hay sospechas fundadas de
taponamiento pericárdico.
Manejo específico del neumotórax a tensión
El neumotórax a tensión se caracteriza por la acumulación
de aire a presión en el espacio pleural. Evita que el pulmón se expanda
correctamente y presiona el corazón y las venas principales. El resultado
favorable depende de la inmediatez del diagnóstico y del tratamiento urgente.
El tratamiento del neumotórax a tensión es la descompresión inmediata con aguja
seguida de toracotomía para la colocación de tubo torácico a la mayor brevedad.
Un proveedor formado puede realizar rápidamente una descompresión con aguja
insertando
un catéter sobre aguja con diámetro 18 a 20 por encima de la tercera costilla
superior del niño (segundo espacio intercostal) en la línea media clavicular. Un
chorro de aire es signo de que la descompresión con aguja se ha realizado
correctamente. Esto indica que
la presión acumulada en el espacio pleural está saliendo.
|
Identificar e intervenir |
La identificación y corrección inmediatas de la causa subyacente de la obstrucción podrían salvar la vida, ya que los niños con shock obstructivo pueden progresar a insuficiencia cardiopulmonar y, de esta afección, rápidamente a paro cardíaco. |
Manejo específico de lesiones ductus- dependientes
Las lesiones ductus-dependientes son un grupo de anomalías cardíacas congénitas.
Estas anomalías derivan en un flujo sanguíneo pulmonar o sistémico que debe
pasar a través de un ductus arterioso permeable.
El flujo sanguíneo pulmonar ductus-dependiente suele incluir una obstrucción
grave en el flujo sanguíneo pulmonar del ventrículo derecho, de forma que todo
el flujo sanguíneo pulmonar fluye desde la aorta a través del ductus arterioso.
Cuando el ductus comienza a cerrarse,
el lactante presenta un cuadro cianótico e hipoxémico importante.
El flujo sanguíneo sistémico ductus-dependiente consiste
en una obstrucción del flujo de salida a través o desde el lado izquierdo del
corazón a la aorta. En estos pacientes, el flujo sanguíneo sistémico debe
proceder del ventrículo derecho y la arteria pulmonar hasta la aorta. En estos
pacientes, cuando el ductus comienza a cerrarse (durante los primeros días o
semanas de vida), se desarrollan
los signos de shock con un grave deterioro en la mala perfusión.
Para cualquier lactante con flujo sanguíneo sistémico o pulmonar ductus-dependiente,
el tratamiento inmediato con una
infusión continua de prostaglandina
E1
(PGE1) para
restablecer la persistencia de la permeabilidad ductal podría salvarle la vida.
Una infusión de PGE1 restablece la persistencia del conducto.
Otras acciones para el manejo de las lesiones obstructivas ductus-dependientes
son :
Ventilación asistida con administración de O2
Ecocardiografía de diagnóstico y consulta al experto para orientar el tratamiento
Administración de agentes inotrópicos para mejorar la contractilidad miocárdica
Administración juiciosa de líquidos para mejorar el gasto cardíaco
Corrección de las alteraciones metabólicas, incluida la acidosis metabólica
Manejo específico de la embolia pulmonar masiva
La embolia pulmonar masiva es un bloqueo repentino en la arteria pulmonar de la
rama principal o grande. Este bloqueo suele estar causado por un coágulo que ha
llegado a los pulmones procedente de otra parte del cuerpo. El bloqueo también
puede obedecer a otras sustancias, como grasa, aire, líquido amniótico,
fragmento de catéter o' material inyectado. El flujo sanguíneo por la
circulación pulmonar al hemicardio izquierdo está obstruido, lo que ocasiona una
disminución en el llenado del hemicardio izquierdo y un gasto cardíaco
inadecuado.
El tratamiento inicial se basa en el mantenimiento,
incluida la administración de O2, la ventilación asistida y la administración de
líquidos si el niño recibe una perfusión deficiente. Consulte a un especialista
que pueda realizar una ecocardiografía, una exploración con tomografía
computerizada (TAC) con contraste IV o una angiografía para confirmar el
diagnóstico. Los anticoagulantes (heparina, enoxaparina) son el tratamiento
definitivo para la mayoría de niños con embolia pulmonar que no están en shock.
Los anticoagulantes no son de acción rápida para eliminar la obstrucción, por
eso considere el uso
de agentes trombolíticos (por ejemplo, activador tisular
del plasminógeno recombinante [rtPA]) en niños con insuficiencia cardiovascular
grave.
La angiografía por TAC es la prueba diagnóstica de elección porque se puede
obtener rápidamente y no requiere angiografía invasiva. Otras pruebas
diagnósticas útiles son gases arteriales, hemograma completo, dímeros D, ECG,
radiografía de tórax, gammagrafía de perfusión- ventilación y ecocardiografía.
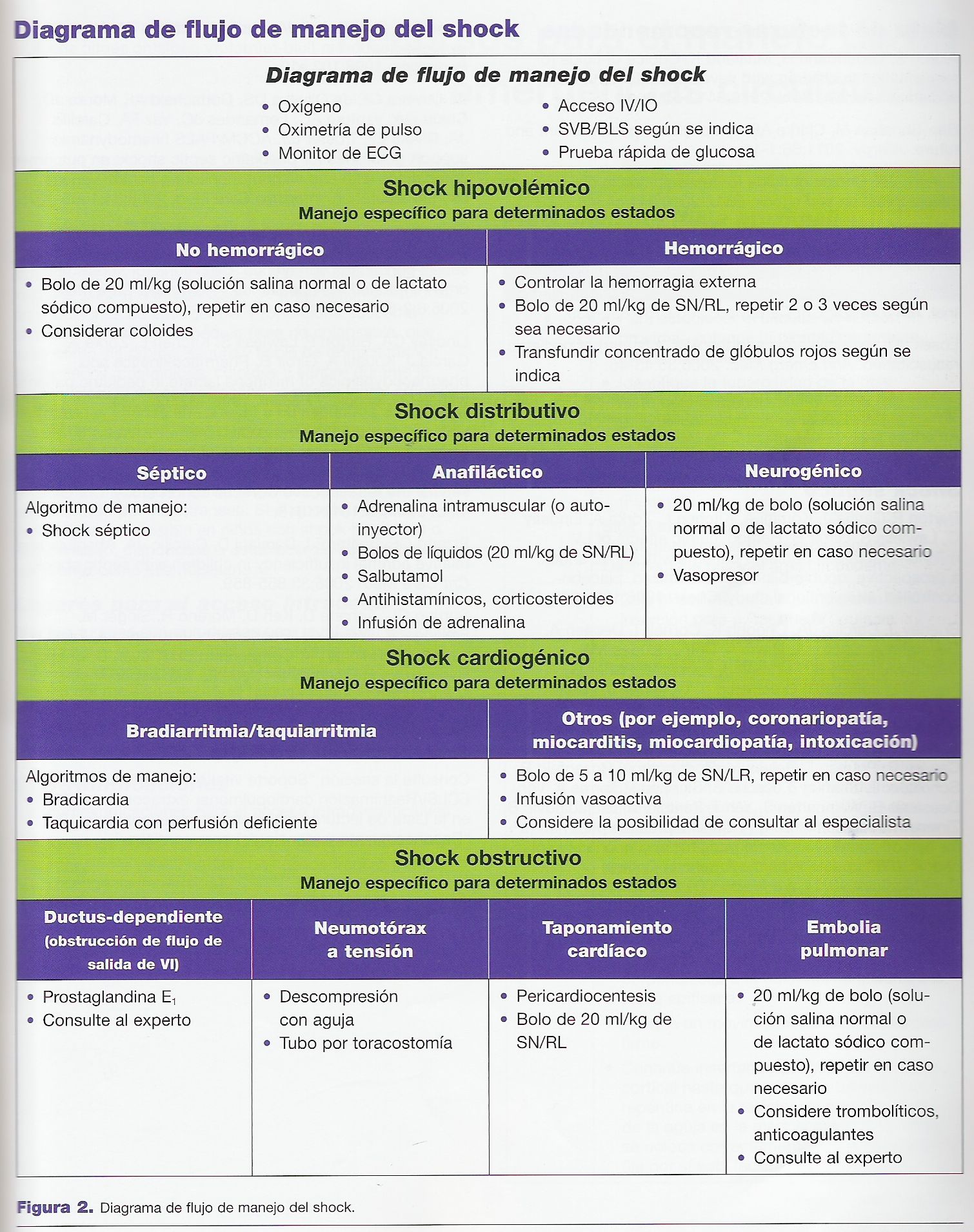
Figura 2.- Diagrama
de flujo de manejo del shock.